Neuartige Screening Methode findet Krankheits-Gene im menschlichen Gehirn Ein Forschungsteam am IMBA – Institut für Molekulare…
Continue ReadingSchlagwort: finanzen
Neue Forschung verweist auf das Krankenhaus der Volksbefreiungsarmee in Wuhan als Ursprungsort der weltweiten Coronavirus-Pandemie
Ein Artikel von Dr. Steven Quay, PhD., Leiter von zwei COVID-19-Therapieprogrammen bei Atossa Therapeutics, Inc. auf…
Continue ReadingStarkes profitables Wachstum bei Sartorius
– Ergebnisse nach neun Monaten: Auftragseingang1 +37,8 Prozent, Umsatz +25,2 Prozent, operative Ertrags1-Marge steigt auf 29,1…
Continue ReadingAVISO: Virtuelle Pressekonferenz – Anyline& Johannes Kepler Universität kündigen KI-Forschungspartnerschaft an
Utl.: Wiener Softwareschmiede & und JKU Institut für Machine Learning starten “few shot learning“ Projekt –…
Continue ReadingAlmirall und die University of Dundee kündigen eine Forschungszusammenarbeit an, um neuartige Medikamente für einen gezielten Proteinabbau zu entwickeln
Almirall, S.A. (ALM) (http://www.almirall.com/) , ein weltweit tätiges biopharmazeutisches Unternehmen, das sich auf die Dermatologie spezialisiert…
Continue Reading
Wie sicherer Wintertourismus möglich ist
MCI: Erste Zwischenergebnisse für aktuelles Forschungsprojekt „COVID-19 – Risikomanagement Wintersaison 2020/2021“ | Gefördert durch die Länder…
Continue ReadingAnanas für die Katze
Mit Enzymen von Ananaspulver unterstützt Placamax, ein neues Produkt von NutriLabs, das Management akuter und chronischer…
Continue ReadingAktuelle Studie inÖsterreich und Deutschland belegt: 40,8 % der Bevölkerung ekelt sich davor, Einkaufswagen im Handel anzufassen!
Über 60% der Menschen wünschen sich eine Reinigung und Desinfektion der Einkaufswagen nach jedem Gebrauch. Nun…
Continue ReadingSteuerliche Forschungsförderung wird umgesetzt
Bescheinigungsstelle nimmt Arbeit auf Forschende Unternehmen können jetzt ihre Forschungsvorhaben zertifizieren lassen. Bevor die steuerliche Forschungszulage…
Continue Reading
Premiere in Wien: Erstmals industrielle Produktion mit 3D-Druck ausÖsterreich möglich
Das Wiener Startup Genera hat ein DLP-Drucksystem auf den Markt gebracht, das im 3D-Druck zu Industrieanforderungen…
Continue Reading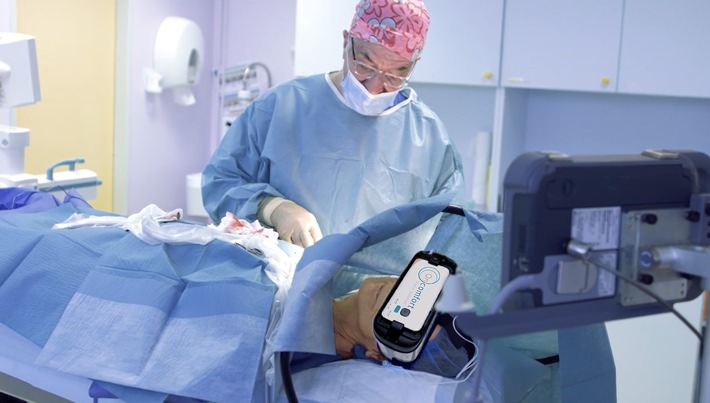
Belgisches Scaleup Oncomfort bringt 10 Millionen EUR für die Weiterentwicklung seiner Digital SedationTM durch Virtuelle Realität mit Debiopharm und Credit Mutuel Innovation auf
Oncomfort, der belgische Erfinder und Marktführer in Digital SedationTM zur medikamentenfreien Schmerzlinderung und Angstlösung bei Patienten,…
Continue ReadingGrifolsübernimmt Alkahest
– Mit der Akquisition wird die Forschung und Entwicklung innovativer Therapien für altersbedingte Krankheiten auf der…
Continue Reading