– Ergebnisse nach neun Monaten: Auftragseingang1 +37,8 Prozent, Umsatz +25,2 Prozent, operative Ertrags1-Marge steigt auf 29,1…
Continue ReadingSchlagwort: pharmaindustrie
Nasus Pharma kündigt erste klinische Daten an, die die Wirksamkeit von Taffix(TM) demonstrieren. Intranasaler antiviraler Schutz gegen SARS-CoV-2 im Super-Spread-Ereignis
Nasus Pharma (https://www.nasuspharma.com/) , ein biopharmazeutisches Unternehmen in Privatbesitz, das ein intranasales (PBI) Produktportfolio auf Pulverbasis…
Continue ReadingAGC Biologics ernennt Luca Alberici zum neuen Generaldirektor/Standortleiter des Standorts Mailand, Italien
AGC Biologics, eine weltweit führendes Unternehmen für biopharmazeutische Auftragsentwicklung und -herstellung (CDMO), hat eine neue Ernennung…
Continue ReadingAufnahme der ersten beiden Patienten in das PRISTINE-Register mit SELUTION SLR(TM) Sirolimus-freisetzendem Ballon
MedAlliance hat am heutigen Tag die Aufnahme der ersten beiden Patienten in das PRISTINE-Register mit SELUTION…
Continue ReadingKedrion ernennt Val Romberg zum CEO
Der altgediente amerikanischen Pharmamanager betrachtet Kedrion als „eine interessante neue Gelegenheit“ Der Verwaltungsrat der italienischen Kedrion…
Continue ReadingAmgen, Cytokinetics und Servier geben Topline-Ergebnisse von GALACTIC-HF bekannt, einer Phase-3-Studie mit Omecamtiv-Mecarbil bei Patienten mit Herzinsuffizienz
– Studie erreicht primären kombinierten Endpunkt der Reduktion von kardiovaskulären Todesfällen oder Herzinsuffizienz-Ereignissen – Studie erreicht…
Continue ReadingAlmirall und die University of Dundee kündigen eine Forschungszusammenarbeit an, um neuartige Medikamente für einen gezielten Proteinabbau zu entwickeln
Almirall, S.A. (ALM) (http://www.almirall.com/) , ein weltweit tätiges biopharmazeutisches Unternehmen, das sich auf die Dermatologie spezialisiert…
Continue ReadingErstes kommerzielles Medikament, dasüber die AJIPHASE-Technologie von Ajinomoto Bio-Pharma Services hergestellt wird, erhält FDA-Zulassung
Ajinomoto Bio-Pharma Services („Aji Bio-Pharma“), ein führender Anbieter von biopharmazeutischen Auftragsentwicklungs- und Produktionsdienstleistungen, freut sich bekannt…
Continue ReadingAufreinigungsspezialist BIA Separations wird Teil von Sartorius
– Kombination schafft einzigartiges Portfolio für Advanced Therapies – BIA wird Sartorius“ Kompetenzzentrum für die Aufreinigung…
Continue ReadingDiscovery Life Sciences startet SpecimenSeq(TM): Genomisch und klinisch annotierte Bioprobensätze zur Beschleunigung der Entwicklung von Flüssigbiopsien und Immuntherapien
Angetrieben durch die Integration der weltweit führenden Bioprobenlösungen von Discovery mit den Sequenzierungs- und Bioinformatikdiensten von…
Continue Reading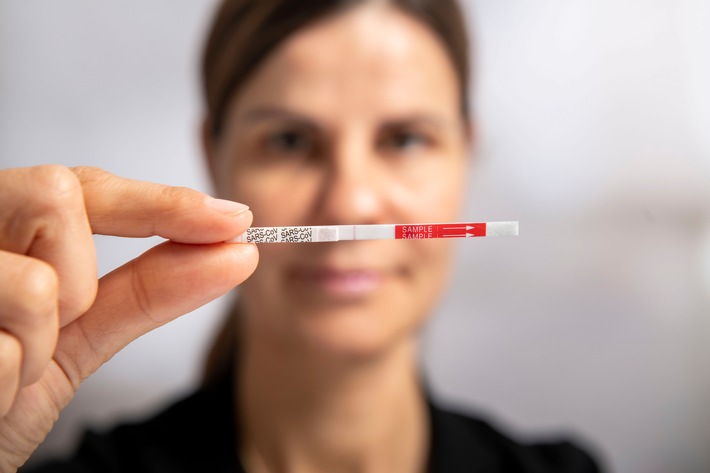
Markteinführung Mitte Oktober 2020: R-Biopharm entwickelt als erstes deutsches Biotech-Unternehmen SARS-CoV-2 Antigen-Schnelltest (FOTO)
– Markteinführung in Deutschland für Mitte Oktober 2020 geplant – Entwicklung und Produktion in Deutschland (Darmstadt)…
Continue ReadingRadius Health& Menarini-Gruppe liefern Elacestrant Update
Zielrekrutierungs-Meilenstein in der Phase-3-EMERALD-Studie erreicht Nutzungsdauerplanung schreitet parallel zum laufenden Monotherapieprogramm der Phase 3 voran Radius…
Continue Reading