Jährlich sterben etwa 353.000 Menschen in Deutschland an
Herz-Kreislauf-Erkrankungen. Damit sind diese hierzulande die
Todesursache Nummer eins.1 Schuld daran ist oft das „schlechte“
Cholesterin.2 Sogenannte Lipoproteine transportieren das Cholesterin
im Blut. Für den Transport des Cholesterins in und aus der Leber
heraus sind LDL (Low-Density Lipoprotein) und HDL (High-Density
Lipoprotein) zuständig. Wird das LDL-Cholesterin während dieses
Prozesses jedoch nicht ausreichend abgebaut, lagert es sich an den
Gefäßinnenwänden an, was zu einer Verengung der Arterie führt. Diese
Verengung kann eine Atherosklerose (Verhärtung der Arterie)
verursachen, die Herz-Kreislauf-Erkrankungen bedingen3 und zum Tod
führen kann.1 Besonders gefährdet sind hierbei sogenannte
Hochrisiko-Patienten. Das sind z.B. Patienten, die aufgrund einer
vorliegenden erblichen Erkrankung – der familiären
Hypercholesterinämie (FH) – besonders hohe LDL-Cholesterin-Werte
haben und bei denen eine herkömmliche cholesterinsenkende Therapie
mit Statinen häufig nicht ausreicht.4
In diesem Geschehen spielt das geheimnisvoll klingende Akronym
PCSK9 (Proprotein-konvertase Subtilisin/Kexin Typ 9) eine
entscheidende Rolle. Dahinter verbirgt sich nämlich ein Protein, das
die Leber daran hindert, das „schlechte“ LDL-Cholesterin aus dem Blut
zu entfernen, was unweigerlich zu erhöhten Cholesterinwerten führt.
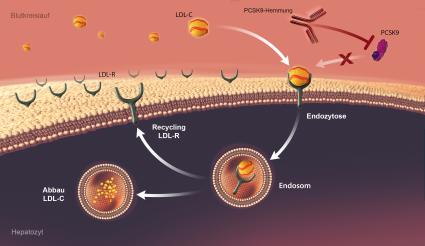
Normalerweise helfen sogenannte LDL-Rezeptoren (Bindungsstellen für
das LDL-Cholesterin an der Leber-zelloberfläche) dem Organ, das
LDL-Cholesterin aus dem Blut herauszufiltern.5 Das PCSK9-Protein aber
stört diesen Prozess, da es die LDL-Rezeptoren bindet, zu deren
Ab-bau in der Leberzelle führt und sie somit für die Aufnahme von
LDL-Cholesterin nicht mehr zur Verfügung stehen. Es gilt also, diese
„Blockade“ zu unterbinden und der Leber ihre natürliche
LDL-Cholesterin-Reinigungsfunktion zurückzugeben.
Gute Mutation gegen schlechtes Cholesterin – die Entdeckung von
PCSK9
Bei der familiären Hypercholesterinämie können Betroffene schon in
jungen Jahren an zu hohen LDL-Cholesterin-Werten leiden.6 Es gilt
jedoch: Je niedriger das LDL-Cholesterin, desto geringer ist das
Risiko für Herz-Kreislauf-Erkrankungen.7 Die Folgen für FH-Patienten
sind dementsprechend fatal: Für über 50 % der Männer mit FH besteht
bereits mit 50 Jahren das Risiko an koronaren Herzkrankheiten zu
erkranken. Bei Frauen um das 60. Lebensjahr betrifft dies mindestens
30 %.8
Durch Studien an Familien mit FH entdeckten Wissenschaftler im
Jahr 2003 das Protein PCSK9 und dessen Bedeutung für den
LDL-Cholesterin-Spiegel.9 Es zeigte sich, dass Mutationen, d. h.
genetische Veränderungen, die Aktivität von PCSK9 verstärken können
und dadurch die LDL-Cholesterin-Werte ansteigen.10 Ein Zusammenhang
zwischen dem Pro-tein PCSK9 und hohen Cholesterinwerten war
hergestellt.
Daraus ergab sich natürlich eine entscheidende Frage: Führt im
Umkehrschluss eine verminderte Aktivität von PCSK9 zu niedrigeren
LDL-Cholesterin-Werten? Schon 2 Jahre später, im Jahr 2005, folgte
die Antwort: Studienergebnisse stützten die Hypothese, dass die
Hemmung von PCSK9 zu einer Senkung von LDL-Cholesterin-Werten führen
kann.11
In nur 10 Jahren zu einem neuen Medikament
Mit der Entdeckung der Mutation war der Grundstein für den Weg zu
einer innovativen Therapieoption gelegt. Für Amgen – das weltweit
größte Biotechnologie-Unternehmen – begann damit ein bedeutendes
Kapitel in der Kardiologie: Die Suche nach einem Antikörper, der
verhindert, dass das Protein PCSK9 die LDL-Rezeptoren der Leber
bindet, deren Abbau und somit auch die Reduktion von LDL-Cholesterin
fördert.
Die Entwicklung neuer Medikamente ist ein langwieriger und
kostenintensiver Prozess. Um Hochrisiko-Patienten jedoch die dringend
benötigte Therapieoption bieten zu können, arbeitete Amgen mit
Hochdruck an der Entwicklung des neuen Wirkstoffs.
In mehreren Schritten identifizierte Amgen einen geeigneten
Antikörper gegen das Protein PCSK9. Dieser durch biotechnologische
Verfahren synthetisch reproduzierte, vollhumane monoklonale
Antikörper fördert den Abbau von LDL-Cholesterin und ist seit Juli
2015 weltweit als erster PCSK9-Hemmer zur Behandlung hoher
Cholesterinwerte in Europa zugelassen.
Amgen – Pionier in der Biotechnologie
Seit seiner Gründung leistet Amgen Pionierarbeit in der
biotechnologischen Produktion von Medikamenten – zunächst in der
Nephrologie, dann in der Onkologie und in der Osteoporose: Bereiche,
in denen das Unternehmen damit neue Maßstäbe setzte. Mit dem neuen
vollhumanen monoklonalen Antikörper steht nun erstmals auch eine sehr
wertvolle biotechnologische Therapieoption für
Herz-Kreislauf-Patienten mit hohen Cholesterinwerten zur Verfügung,
die das Leben vieler Menschen verändern wird.
„Der Schlüssel zur Heilung liegt in uns selbst!“ Das Credo des
1980 gegründeten Unternehmens drückt aus, dass sich in der
menschlichen Biologie Potenziale entdecken lassen, um schwerwiegende
Erkrankungen erfolgreich behandeln zu können. Dabei fokussiert sich
Amgen vor allem auf Therapiegebiete, in denen ein bislang ungedeckter
bzw. nicht ausreichend gedeckter Behandlungsbedarf besteht. Die
PCSK9-Entdeckungsgeschichte belegt das eindrucksvoll.
Referenzen
1 Nichols M, Townsend N, Scarborough P, Rayner M. European
Cardiovascular Disease Statis-tics 2012
2 Akram ON, Bernier A, Petrides F, et al. Beyond LDL Cholesterol, a
New Role for PCSK9. Arte-rioscler Thromb Vasc Biol. 2010;30:1279-1281
3 National Human Genome Research Institute. Learning About Familial
Hypercholesterolemia. http://www.genome.gov/25520184. Letzter Aufruf:
August 2015
4 Nordestgaard BG, Chapman MJ, Humphries SE, et al. Familial
hypercholesterolaemia is un-derdiagnosed and undertreated in the
general population: guidance for clinicians to prevent coronary heart
disease. Eur Heart J. 2013;34:3478-3490
5 Qian YW, Schmidt RJ, Zhang Y, et al. Secreted PCSK9 downregulates
low density lipoprotein receptor through receptor-mediated
endocytosis. J Lipid Res. 2007;48:1488-1498
6 Klose G, Laufs U, März W, Windler E. Familial
Hypercholesterolemia: Developments in Diag-nosis and Treatment. Dtsch
Arztebl Int. 2014;111:523-529
7 Cholesterol Treatment Trialists“ (CTT) Collaborators. Efficacy
and safety of cholesterol-lowering treatment: prospective
meta-analysis of data from 90,056 participants in 14 randomised
trials of statins. Lancet. 2005;366:1267-1278
8 Marks D, Thorogood M, Neil HA, Humphries SE. A review on the
diagnosis, natural history, and treatment of familial
hypercholesterolaemia. Atherosclerosis. 2003;168:1-14
9 Abifadel M, Varret M, Rabes JP, et al. Mutations in PCSK9 cause
autosomal dominant hyper-cholesterolemia. Nat Genet. 2003;34:154-156
10 Park SW, Moon Y, Horton JA. Post-transcriptional regulation of
low density lipoprotein receptor protein by proprotein convertase
subtilisin/kexin type 9a in mouse liver. J Biol Chem.
2004;279:50630-50638
11 Cohen J, Pertsemlidis A, Kotowski IK, et al. Low LDL cholesterol
in individuals of African de-scent resulting from frequent nonsense
mutations in PCSK9. Nature Genetics. 2005;37:161-165
Pressekontakt:
Dr. Corinna Jacob, eMail: corinna.jacob@amgen.com, Telefon:
089-149096-1604